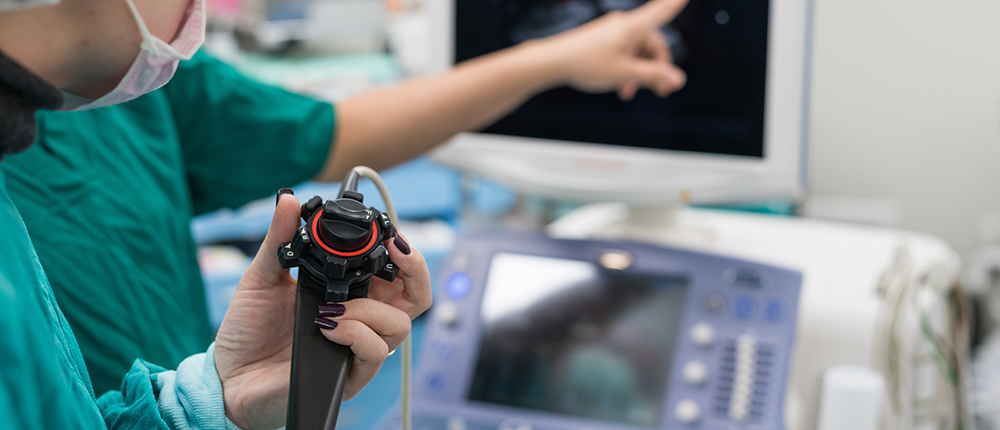
担当医師
山下 英治(循環器内科第三部長)
毛見 勇太
福士 朋子
循環器内科第三部(心エコー部門)では、主に下記の業務を実施しています。
心エコー検査
経食道心エコー検査や、ドブタミン等の薬剤を用いた負荷心エコー検査などを実施しています。
ドブタミン負荷心エコー検査は、低流量重症大動脈弁狭窄症の手術適応の判断に有効であり、当院では積極的に実施しています。
なお、通常の経胸壁心エコー・血管エコー検査は、生理検査課の検査技師が担当し、年間10,000件を超える経胸壁心エコー検査及び年間1,200件を超える血管エコー検査を実施しています。
経食道心エコー検査

- 胃カメラよりもやや太い管に超音波センサーが付いた機器を用いて、心臓の画像を描出します。
- 当院では咽頭麻酔と静脈麻酔(全身麻酔)を使用します。胃カメラが苦手な患者様でも、最小限の苦痛で検査可能です(所要時間10~30分)。
- 食道は直接心臓に接している部位です。そのため、経胸壁からの超音波検査により、明瞭な心臓の画像が得られます。
- 検査結果は、不整脈治療(心房細動アブレーション)前の血栓評価や、弁膜症・成人先天性心疾患の手術適応評価、術式決定のための精密検査等に用いられます。
- 開心手術や経カテーテル大動脈弁置換術(TAVR)の術中モニタリング等にも用いられます。
- 当院では患者の苦痛低減のため、全例静脈麻酔を用いて検査を行っています。
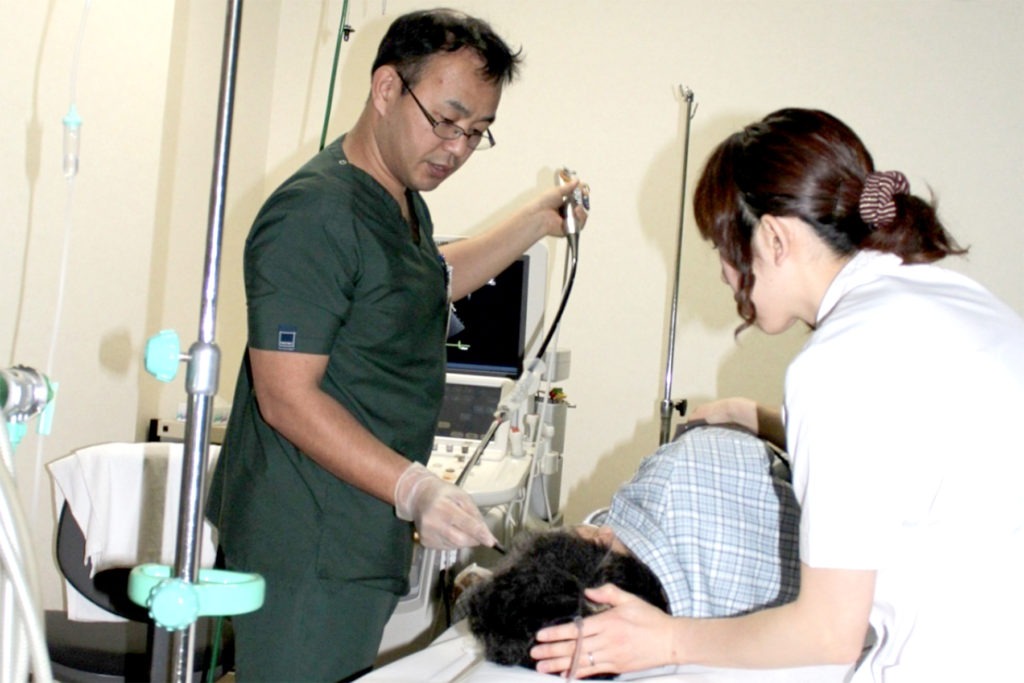
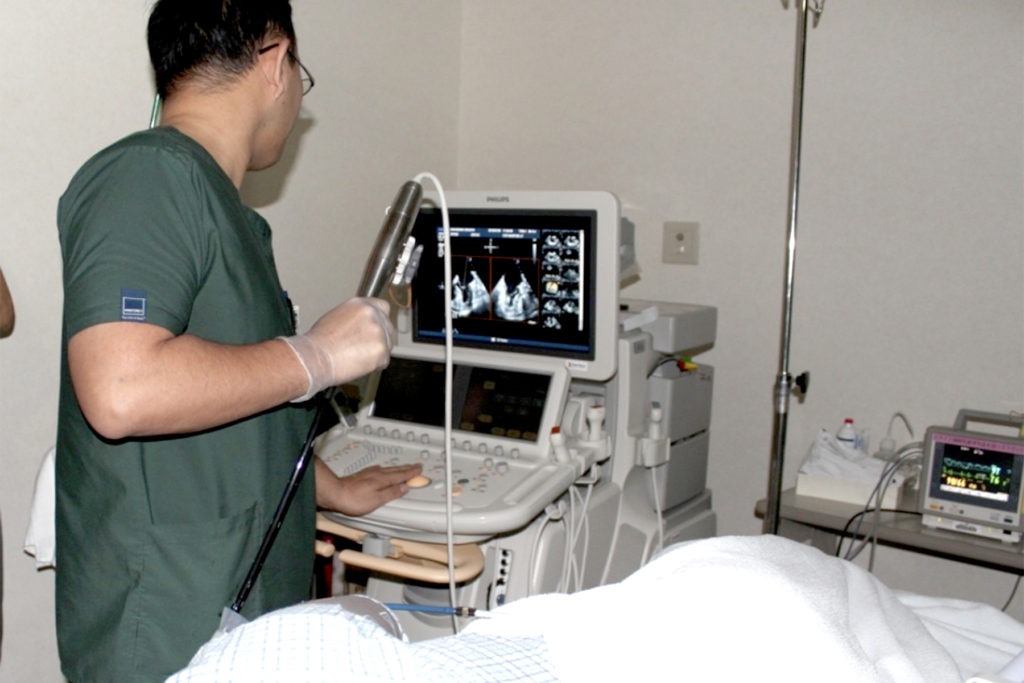
当院の経食道心エコー検査数
| 年度 | 2016 | 2017 | 2018 | 2019 | 2020 | 2021 | 2022 | 2023 |
| 件数 | 1,183 | 1,079 | 1,130 | 1,235 | 993 | 777 | 1,043 | 974 |
弁膜症外来

弁膜症患者の手術適応評価および術後経過観察を行う弁膜症外来を開設しています。
経胸壁心エコー検査での評価を基に、経食道心エコー検査・負荷心エコー検査・CT・MRI・心肺運動負荷試験等のデータを併せ、患者の治療方針を決定しています。また当院は、TAVR/TAVIの認定施設であり、治療適応患者を積極的に受け入れています。(http://j-tavr.com/facility.html)
判断が難しい症例では、循環器内科・心臓血管外科・麻酔科その他スタッフを交えたカンファランスを行い、治療方針を検討しています。
成人先天性心疾患外来
近年の医療レベル向上により、複雑心奇形の生存率が著しく向上しています。これにより、先天性心疾患を抱える方が成人に達し、社会生活を営むケースも増えています。現在では、成人に達した有病者数が、18歳未満の有病者数を上回っています。
当院では、地域の診療所や病院でフォローされている患者様のうち、次のような方の受け入れを行っています。
- カテーテル治療適応対象かつ未治療の方(心房中隔欠損・動脈管開存症等)
- 小児期に手術を受けた後、再手術が必要な方(ファロー四徴症等)
- 成人期に手術が必要な可能性がある方(修正大血管転位・エブスタイン奇形等)
- 小児科で先天性心疾患の治療を受け、成人の循環器内科に移行した方
これらの患者様が検査や治療、手術を必要とする場合には、心臓の状態管理を行います。また、再手術や複雑な症例の場合、県立小児医療センターを交えた合同カンファランスを行い、手術・治療方針を決定しています。さらに、当施設で対応が困難な場合は、適切な専門医療機関への紹介も行います。
第二・第四金曜日の午後に外来診療を行っています。なお予約制ですので、受診希望の方はあらかじめ電話でお問い合わせください。
成人先天性心疾患専門医連携修練施設

当院は、日本成人先天性心疾患学会から成人先天性心疾患専門医の連携修練施設に認定されています。(https://www.jsachd.org/specialist/list-facility/kanto/)
本制度は、成人先天性心疾患を診療できる専門医の育成を目的とするものです。そのため、成人先天性心疾患の診療実績を多く有する施設が認定されています。
(https://www.jsachd.org/specialist/list-specialist/)
経皮的心房中隔欠損閉鎖術・経皮的動脈管開存閉鎖術
心房中隔欠損(ASD)や動脈管開存症(PDA)は、通常では小児期に治療されることが多いです。しかし、成人期に発見されることも多く、心不全や不整脈の原因にもなっています。
近年、これらの疾患に対するカテーテル治療が普及してきています。カテーテル治療は、開胸が不要で、患者様の負担が軽減可能な治療法です。そのため県内でも、成人ASD・PDA患者への治療が実施施設が望まれていました。
2019年、当院は小児循環器領域のカテーテル治療の学会であるJPICと、成人循環器領域のカテーテル治療の学会であるCVITにおいて、経皮的ASD閉鎖術施行施設・経皮的PDA閉鎖術施行施設に認定されました。
(http://www.jpic-meeting.org/cathe/asd.shtml#02)
(http://www.jpic-meeting.org/cathe/pda.shtml#02)
ASDに対しては、Amplatzer Septal Occluder(ASO)及びFigulla Flex-Ⅱ(FF-Ⅱ)の2種類の閉鎖栓を、PDAに対してはAmplatzer Duct Occluderを用いて手術を施行しています。
今後も安全かつ患者様の負担の軽い手術・治療に取り組んでいきます。


臨床研究
心エコー部門では、臨床を踏まえた研究発表を盛んに行っています。現在も以下に示す研究等を進めています。
- 成人先天性心疾患罹患率や経食道エコー検査による診断精度の向上に関する研究
- 心房細動の血栓リスク層別化に関する研究
- Watchman左心耳閉鎖デバイス適応に関する研究
- 左心耳血栓とsludgeとの鑑別法
- 大動脈弁狭窄症例のTAVR後の症状別予後や予後予測因子解析
- 卵円孔開存症診断法の開発 等